Category: Bản tin
Các tin tức cập nhật của Viện Tế bào gốc.
-
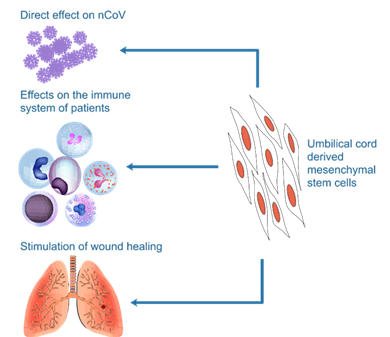
Tiềm năng sử dụng công nghệ của Viện Tế bào gốc trong quy trình điều trị COVID-19
Sử dụng tế bào gốc trong điều trị bệnh Covid-19 không còn là ý tưởng mới. Đến hôm nay đã có 69 nghiên cứu thử nghiệm lâm sàng sử dụng tế bào gốc điều trị Covid-19 đăng kí trên trang clinicaltrials.gov. Vậy các công nghệ của Viện Tế bào gốc nghiên cứu, phát triển có…
-
VIỆN TẾ BÀO GỐC,TRƯỜNG ĐH KHOA HỌC TỰ NHIÊN, ĐHQG-HCM MỞ CÁC CHƯƠNG TRÌNH ĐÀO TẠO CHUYÊN SÂU
Nhận thấy nhu cầu được nâng cao trình độ tay nghề của các đối tượng học viên đã tốt nghiệp, đã đi làm ở các trung tâm, phòng thí nghiệm và trường học trên các nội dung như Kỹ thuật nuôi cấy tế bào, tế bào gốc, kỹ thuật phân tích phân tách tế bào,…
-
THÔNG BÁO HỦY CUỘC THI SÁNG TẠO TẾ BÀO GỐC-STEM CELL INNOVATION NĂM LẦN 2020
Hiện nay, dịch bệnh Covid 19 vẫn còn đang diễn biến phức tạp. Nhằm đảm bảo cho các bạn học sinh, sinh viên tham gia và thực hiện theo chỉ đạo quốc gia về phòng, chống dịch, Viện Tế bào gốc xin thông báo hủy tổ chức cuộc thi Sáng tạo tế bào gốc –…
-
STEM CELL SUMMER TOUR_ CHƯƠNG TRÌNH KẾT NỐI VÀ LAN TỎA NIỀM ĐAM MÊ KHOA HỌC TẾ BÀO GỐC
Mùa hè năm nay, chương trình Stem Cell Summer Tour 2020 đã quay trở lại thu hút nhiều sự quan tâm, đăng kí của nhiều bạn học sinh, sinh viên cũng như các công ty, trường đại học … Sau 1 tháng diễn ra, chương trình đã giới thiệu, hướng dẫn tham quan Viện Tế…
-
Thuốc tế bào gốc – Đột phá công nghệ của Viện Tế bào gốc
Viện Tế bào gốc bắt đầu tiếp cận công nghệ thuốc tế bào gốc từ năm 2012. Đến nay, Viện Tế bào gốc đã làm chủ các công nghệ cốt lõi của công nghệ thuốc tế bào gốc. Các sản phẩm thuốc tế bào gốc của Viện thường sử dụng tế bào gốc từ mô…
-
VIỆN TẾ BÀO GỐC CUNG CẤP DỊCH VỤ SÀNG LỌC HOẠT TÍNH SINH HỌC TRÊN TẾ BÀO NGƯỜI VÀ ĐỘNG VẬT
Hiện nay, đánh giá hoạt tính sinh học của cao chiết, dịch chiết, chất, hợp chất, protein… lên tế bào người và động vật là những thí nghiệm quen thuộc, thường xuyên trong các phòng thí nghiệm, đặc biệt trong các nghiên cứu phát hiện thuốc. Các hoạt tính sinh học thường được đánh giá…
-
[THÔNG BÁO] STEM CELL SUMMER TOUR 2020
Ban tổ chức chương trình Stem Cell Summer Tour 2020 xin thông báo đến các bạn học sinh – sinh viên như sau: 1️⃣ Chương trình vẫn tiếp tục diễn ra như kế hoạch cho đến khi có thông báo tiếp theo 2️⃣Các bạn học sinh – sinh viên tham gia chương trình cần đảm…
-
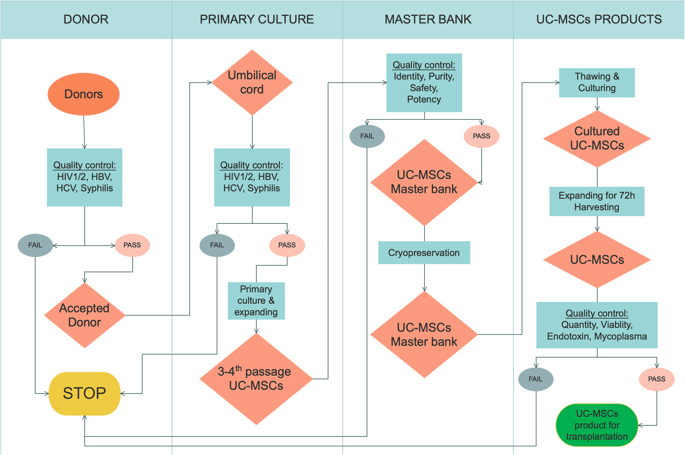
CÔNG NGHỆ SẢN XUẤT TẾ BÀO GỐC TRUNG MÔ TỪ MÔ DÂY RỐN NGƯỜI – CÔNG NGHỆ UC-SCI
Công nghệ sản xuất tế bào gốc trung mô từ mô dây rốn người (UC-SCI) của Viện Tế bào gốc là công nghệ toàn diện và đồng độ cho sản xuất tế bào gốc quy mô nhỏ (trong chai nuôi cấy) và lớn (trong bioreactor).
-
Cấy ghép tế bào gốc trung mô đồng loài để điều trị bệnh thiếu máu không tái tạo: một nghiên cứu phase II đa trung tâm
Thiếu máu không tái tạo (Aplastic anemia – AA) là chứng suy tủy xương được đặc trưng bởi chứng giảm tủy và cạn kiệt các tế bào tiền thân tạo máu. Quá trình phá hủy các tế bào tiền thân tạo máu qua trung gian miễn dịch đã được khẳng định bằng các nghiên cứu…
-
Buồng trứng được tạo ra từ công nghệ in 3D có thể phục hồi khả năng sinh sản trên chuột
Bây giờ bạn có thể in các cơ quan bằng công nghệ in 3D. Trên thực tế, các cấu trúc buồng trứng có thể được in theo cách tương tự để tạo ra một buồng trứng giống thiết kế của buồng trứng thật. Một nghiên cứu được thực hiện tại Trường Y khoa Feinberg, Trường…